Modificat 14.4.2012
QUÍMICA. Atom. Taula
periòdica. Enllaç
Cal
introduir modificacions: mirar impressió paper
Mireu els següents vídeos:
|
|
ok-01. quimica animacion CSIC.mp4 La
química y la vida.wmv
La
química y nosotros.wmv
Vivir
sin química.wmv
|
|
00 |
Química.
ok-01. quimica animacion CSIC.mp4 ok-02.¿De qué estamos hechos_.mp4 ok-03.potencias de 10 (esp).mp4 OK-03a-pluma-martillo-luna-apollo15.mp4 ok-04. Size Comparison - From a
Molecule to a Galaxy In One Single Shot .mp4 |
|
01 |
Atom. Models atòmics
ok-05.
Atomo-part.subatomica-radioactividad.mp4 ok-06. Experimento de
Rutherford-subtitulado.mp4 ok-07. MODELOS ATÓMICOS.mp4 Isotopes.mp4 |
|
02** |
Canvis d'estat
ok-Canvis d'estat de l'aigua
OKOKOK.divx ok-physical changes heating and
cooling.divx |
|
03*** |
Enllaç
Ionic and covalent bonding
animation.mp4 |
|
|
Taula periòdica
ok-Mendeleiev_una_taula_digna_d_un_nobel.flv Chemical Party.mp4 |
Links
|
Proyecto Ed@d . Ministeri de Educación.
Física y química 3º de ESO
http://recursostic.educacion.es/secundaria/edad/3esofisicaquimica/index.htm |
Concurso.cnice.mec.es. Aplicación web
interactiva de los temas de química 3r ESO.
http://concurso.cnice.mec.es/cnice2005/35_las_reacciones_quimicas/curso/index.html
|
|
Nou positró 3. Ed.
Vicens Vives http://centres.vicensvivesdigital.cat/35099/course/format/vvives/index.php?id=18 |
|
llibrewebsantillana |
|
Educaplus.org. |
|
yTeach.co.uk is the eLearning
Superstore where you can buy and use high-quality teaching and learning
resources for Science and Maths. |
Bibliografia
|
OKOK-Gradui's ara (pdf en disc dur) Àmbit de les
Matemàtiques, de la Ciència i de la Tecnologia 6_el_mon_invisible_04.pdf |
|
Alucina con la química! Robert winston. SM ISBN:978-84-675-2059-0 |
|
Solucionari. Física i química 3ESO. Biblioteca del professorat. Grup Promotor Santillana. Prjecte la Casa del saber. ISBN: 13978-84-7918-155-0 |
|
Chemistry for You. Lawrie Ryan. Nelson Thornes |
¡
1. ÀTOM-TAULA PERIÒDICA-ENLLAÇ
1.1. Què és la química?
|
Vídeos: ok-01. quimica animacion CSIC.mp4 La
química y la vida.wmv
La
química y nosotros.wmv
Vivir sin química.wmv 03a. Democritus atomic theory.divx |

La química és la ciència que estudia la matèria.
La química estudia:
1) Com és la matèria (la composició, estructura, i propietats de la matèria)
veure vídeo: 03a. Democritus atomic theory.divx
2) Quins canvis fa la matèria (canvis que la matèria experimenta durant les reaccions químiques).
Si mirem al nostre voltant, què veiem?
La resposta és: Química.
La Química és a tot arreu: la roba que portem, allò que mengem, l’aire que respirem, els nostres cossos…
Tot és fet de matèria, i tota la matèria està formada per àtoms i molècules; per tant, tot és Química.
1.2 Breu història de la química?
|
|
1.2.1.
Orígens. El foc Els orígens de la Química es remunten als de la humanitat. El primer químic, sense saber-ho, va ser el ser humà primitiu quan va
aconseguir controlar i utilitzar el foc,
produït per la reacció química de la
combustió. El foc va millorar considerablement la qualitat de vida, en qüestions
com la cocció d’aliments, la fabricació d’eines, la seva utilització com a
font de calor. A més a més, va possibilitar el desenvolupament posterior de
la ceràmica i la metal·lúrgia del coure, del bronze i del ferro. Gràcies al foc l'home ja no depenia de la llum de Sol per les nits.
El foc va possibilitar que els tribus i famílies es reunissin per parlar de
les seves coses, per explicar històries i va ajudar a crear el sentiment de comunitat que és una de
les claus de l'èxit de l'espècie humana. |
|
1.2.2.
La Alquímia Des de feia molts segles i fins al segle XVII la química va estar
dominada per l’Alquímia. L'alquímia era una doctrina. Una filosofia, una espècie de religió.
Des d'un punt de vista actual, és una pseudociència sense base científica.
que pretenia explicar com una substància es podia transformar en una altra, Un dels objectius principals era la recerca de la pedra filosofal, que hauria de
permetre transformar qualsevol metall en or. En general, els alquimistes creien que tota la matèria estava
composta per quatre elements: terra, aire, aigua i foc. Els alquimistes eren
una mescla de bruixot i científic primitiu. En el plànol espiritual, els alquimistes havien de transmutar
(canviar) la seva pròpia ànima abans de transmutar els metalls. L’alquímia
era com una mena de religió mística. Val a a dir al seu favor que els alquimistes van desenvolupar molts
processos químics, van descobrir noves substàncies químiques i es van
perfeccionar les eines de treball. científic en aquest camp. |
|
Als laboratoris alquimistes es buscava la pedra fi losofal, un mètode
hipotètic que hauria de permetre transformar qualsevol metall en or.
Els alquimistes xinesos buscaven un elixir que pogués allargar la vida
i fins i tot conferir la immortalitat.
1.2.3.
La química com a ciència
La química comença a ser una ciència quan aplica el mètode científic
per fer nous descobriments. La Química es va convertir en una ciència al segle
XVII gràcies a Robert Boyle, pioner
en aplicar el mètode científic en els seus estudis.
|
|
Antoine Laurent Lavoisier (1743-1794) va
tenir un paper fonamental i és considerat el pare de la Química moderna. Va
fer experiments rigorosos mesurant acuradament les quantitats utilitzades. - És el pare de la llei de conservació de la massa (La massa dels productes d'una reacció
química és igual a la massa dels reactius de la reacció) - va establir el concepte d’element químic - va contribuir a fixar un sistema de nomenclatura per posar ordre a
la quantitats de noms diferents que hi havia per anomenar les mateixes substancies.
Per exemple l'àcid sulfúric s'anomenava oli de vidriol, esperit de vidriol,
licor de vidriol i això dificultava molt l'avenç de la ciència.. |
Que és
el mètode científic?
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=1§ion=3
|
Els científics que estudien la natura utilitzen el mètode científic
per arribar a conclusions rigoroses. Un científics no només ha de tenir unes idees brillants. A més les
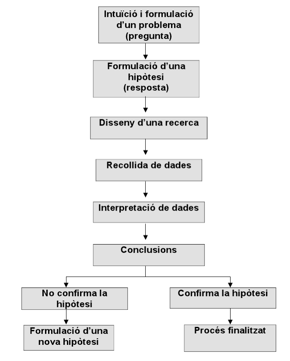
han de poder demostrar amb experiments. Les etapes de què consta l'estudi seguint el mètode científic són: - Plantejament del problema. - Recerca d'informació. - Formulació d'una hipòtesi que expliqui el
problema. - Es fan experiments i es recolleixen
dades. - Anàlisi de les dades ( mirem si les dades
confirmen la nostra hipòtesi). - Obtenció de resultats i conclusions. |
|
|
|
|
|
|
Activitats Moodle Nou
Positro 3 http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=1§ion=3 |
|
1) Ordena. Les etapes mètode científic 2) Resumeix. La investigació científica Qüestió 1.Explica què és
el mètode científic i quines són les seves etapes. 3) Raona. L'experimentació i la teoria
científica Qüestió 2. Els
experiments són observacions controlades que donen molta informació als
científics. No obstant això, no sempre són possibles. Explica algun cas en el
qual els científics no puguin realitzar experiments |
|
Exemple de mètode científic:
NOTA MIF:
1) per fer aquesta activitat
pot utilitzar-se una bola de porespan i una bola d'acer que es deixaran caure
totes dues alhora.
2) Convé veure el vídeo: "experimento Pluma-Martillo" (efectuat en la superfície lunar per l'astronauta Scott de la misió Apollo 15) OK-03a-pluma-martillo-luna-apollo15.mp4 |
|
Volem estudiar si la velocitat de caiguda lliure
dels cossos depèn de la seva massa. Per a això, deixem caure,
des d'una mateixa altura un guix i una fulla de paper. Observem que el guix
arriba molt abans que el paper al sòl. Si mesurem la massa del guix, veiem que
aquesta és major que la massa del paper.
Formulació d'hipòtesi
Després de les observacions, el científic es planteja el
com i el perquè del que ha ocorregut i formula una hipòtesi. Formular una
hipòtesi consisteix a elaborar una explicació provisional dels fets observats i
de les seves possibles causes.
Exemple: Podem formular, com a
hipòtesi, el següent raonament: "Cau amb major velocitat el cos que
posseeix major massa".
Experimentació
Una vegada formulada la hipòtesi, el científic ha de
comprovar si és certa. Per a això realitzarà múltiples experiments modificant
les variables que intervenen en el procés i comprovarà si es compleix la seva
hipòtesi.
Experimentar consisteix a reproduir i observar diverses
vegades el fet o fenomen que es vol estudiar, modificant les circumstàncies que
es considerin convenients.
Durant l'experimentació, els científics acostumen a
realitzar múltiples mesures de diferents magnituds físiques. D'aquesta manera
poden estudiar què relació existeix entre una magnitud i l'altra.
Exemple: Si llancem el guix al
costat d'una fulla de paper arrugada, veiem que arriben al sòl pràcticament al
mateix temps. Si seguim aquesta línia d'investigació i llancem una fulla de
paper arrugada i una altra fulla sense arrugar des de la mateixa altura, veiem
que la fulla arrugada arriba molt abans al sòl.
Emissió de conclusions
L'anàlisi de les dades experimentals permet al científic
comprovar si la seva hipòtesi era correcta i donar una explicació científica al
fet o fenomen observat.
L'emissió de conclusions consisteix en la interpretació
dels fets observats d'acord amb les dades experimentals.
De vegades es repeteixen certes pautes en tots els fets i
fenòmens observats. En aquest cas pot enunciar-se una llei. Una llei científica
és la formulació de les regularitats observades en un fet o fenomen natural. En
general, s'expressa matemàticament.
Les lleis científiques s'integren en teories. Una teoria
científica és una explicació global d'una sèrie d'observacions i lleis
interrelacionades.
Exemple: A la vista dels resultats
experimentals, es pot concloure que no és la massa la que determina que un
objecte caigui abans que un altre a la Terra; més aviat, serà la forma de
l'objecte la determinant. Com a comprovació del nostre resultat deduïm que la
nostra hipòtesi inicial era incorrecta. Tenim, per exemple, el cas d'un
paracaigudista: la seva massa és la mateixa amb el paracaigudes obert i sense
obrir; no obstant això, cau molt més ràpid si el paracaigudes es troba tancat.
1.3. Què és la matèria?
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=2§ion=3
Vídeos: química matèria.
ok-01. quimica animacion CSIC.mp4 ok-02.¿De qué estamos hechos_.mp4 ok-03.potencias de 10 (esp).mp4 ok-04. Size Comparison - From a Molecule to a Galaxy In One Single Shot (Annotations On).mp4 |
La química és la ciència que estudia la matèria però què és la matèria?.
Tot el que hi ha al teu voltant és matèria. El llibre que estàs llegint o l'aire que respires, encara que no el puguis veure, és matèria.
|
Matèria és tot allò que té massa i que ocupa un volum. |
|
La matèria està composta
per molècules, les quals es formen per la unió d'àtoms. |
Com ja saps, la matèria pot presentar-se a la natura en algun d'aquests tres estats d'agregació: sòlid, líquid o gas. Això ja ho vas estudiar en cursos anteriors
|
|
|
ÀTOM Unitat més petita d’un element químic que manté la seva identitat. |
|
|
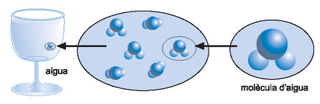
MOLÈCULA Partícula formada per àtoms, que s’uneixen a través d’enllaços químics. ( perquè ho entenguis si veus una molècula d'aigua l'àtom és una bola la molècula és la unió de diferents boles ) |
|
|
A la majoria dels àtoms no els agrada la solitud, de manera que s'uneixen a uns altres, en ocasions idèntics a ells. |
|
|
Els materials formats per un sol tipus d'àtom es denominen ELEMENTS |
|
|
Altres vegades prefereixen unir-se a àtoms d'un tipus diferent. Quan àtoms de tipus diferents s'uneixen, formen materials anomenats COMPOSTOS |
|
|
|
Elemental, benvolgut Watson!..........
Com ja hem dit, els elements estan formats per un sol tipus d'àtoms. Així, per exemple, l'or i la plata són elements. L'or és un element, consta només d'àtoms d'or (Au). La plata també és un element, consta només d'àtoms de plata (Ag) .
L'aigua H2O és un compost perquè està formada per àtoms d'hidrogen H i d'oxigen O.
L'amoníac NH3 és un compost perquè està format per àtoms d'hidrogen H i de nitrogen N.
|
|
Activitats Moodle Nou Positró http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=5 |
|
1) Classifica. Elements i compostos |
|
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=5
ARTÍCULO: Muy
Interesante. Moléculas que cambiaron el Mundo
http://issuu.com/profefaro/docs/m.i.mol.camb.mun
|
1.4. Classificació de la matèria
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=3§ion=3
Segons la seva composició i aparença la matèria es pot classificar de la següent manera:
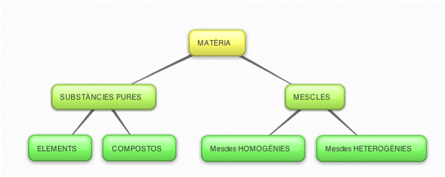
Fet amb https://bubbl.us/
Substància pura és cadascun dels tipus de matèria que té una composició definida i unes propietats característiques i invariables.
Per què ho entenguis, una substància pura està formada per un únic tipus de
substància. Per exemple, L'or (Au), la plata (Ag), l'aigua (H2O),
l'amoníac (NH3) son substàncies
pures.
L'or està format únicament per àtoms d'or,
l'aigua està formada únicament per molècules d'aigua.
Una substància
pura no es mai una mescla de diferents substàncies.
Les substàncies pures es subdivideixen en: elements i
compostos. Abans hem vist que:
Elements Són els materials que estan formats per un sol tipus
d'àtom. Com l'or (Au) o la plata (Ag),
Compostos. Són els materials que estan formats per diferents tipus d'àtoms. Com l'aigua (H2O) o l'amoníac (NH3).
Mescla és un tipus de matèria que està formada per dues o més substàncies pures diferents.
Són mescles, per exemple: el vi, la llet, el granit, l'aire o l'aigua de mar.
|
|
|
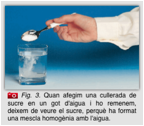
Mescles homogènies
En una mescla homogènia les partícules que la componen són tan petites que no podem observar-les ni amb l'ull nu ni amb cap mitjà òptic (lupa o microscopi)
Així, per exemple, l'aigua del mar o aigua
amb sucre dissolt és una mescla homogènia, perquè no podem distingir les
partícules d'aigua de les partícules de les diferents sals que hi té dissoltes.
Mescles heterogènies
En una mescla heterogènia les partícules de les diferents substàncies que la componen poden observar-se a cop d'ull o amb instruments òptics de pocs augments.
Aquest és el cas del granit, del qual podem
observar a primera vista els tres minerals que el formen (fig. 2).
Un suc de taronja o una sopa de fideus són mescles heterogènies perquè podem
observar a simple vista diferent parts que les formen.


Activitat
interactiva
|
Concurso.cnice.mec.es.
Aplicación web interactiva de los temas de química 3r ESO ELEMENTO, COMPUESTO O MEZCLA? http://concurso.cnice.mec.es/cnice2005/35_las_reacciones_quimicas/curso/em_ex02.html |
|
|
TRUC per tenir les coses
clares: |
Els elements i compostos
tenen sempre una fórmula química
Exemples
|
Oxigen O2 |
Aigua H2O |
|
Heli He |
Quars SiO2 |
|
Nitrogen N2 |
Clorur de sodi NaCl |
|
Ferro Fe |
Àcid sulfúric H2SO4 |
Observeu que:
- en els elements (els de la primera columna) només apareix un símbol O
/He / N / Fe. Això vol dir que estan format per un sols tipus d'àtom.
- en els compostos(els de la segona columna) apareix més d'un símbol H
i O / Si i O / Na i Cl / H, S i O /. Això vol dir que estan format per més d'un
tipus d'àtom.
Teniu en compte que tant elements com compostos són substàncies pures ( no estan fets mesclant diferents substàncies)
Les mescles no tenen una fórmula
química.
No hi ha cap formula per al granit, ni per a l'acer, ni per al suc de taronja o la llet.
Són mescles, no tenen una composició fixa. La llet pot tenir un 2% de greix o un 1,5% i segueix sent llet.
En canvi, l'aigua H2O (substància pura), per exemple, ha de tenir sempre dos àtoms d'H per cada àtom d'O.
Si tingués dos àtoms d'H i dos àtoms d'O seria H2O2 ja no seria aigua, seria aigua oxigenada que us podem assegurar que no serveix per beure.
1.5. Canvis d'estat
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=2§ion=3
VIDEOS: Canvis d'estat
ok-Canvis d'estat de l'aigua OKOKOK.divx ok-physical changes heating and cooling.divx |
Com ja saps, la matèria pot presentar-se a la natura en algun d'aquests
tres estats d'agregació: sòlid, líquid o gas.
Els estats d'agregació no són permanents. Si sotmetem la matèria a
variacions de temperatura o de pressió, pot passar d'un estat a l'altre.
Aquesta transformació rep el nom de canvi
d'estat.
Per exemple, si agafem un tros de glaç i
l'escalfem, es fondrà i es convertirà en aigua líquida i, si continuem
escalfant-lo, es transformarà en vapor d'aigua.
El procés també pot donar-se a l'inrevés, ja
que si refredem el vapor d'aigua, aquest es condensarà en aigua líquida i,
després, se solidificarà en forma de glaç (fig. 3).
Aquests són els canvis d'estat que es poden donar a la matèria segons
donem calor o traiem calor (escalfem o refredem)
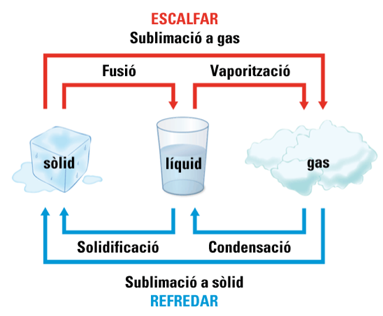
Atenció: també podem causar acnvis d'estat de diferents substàncies
augmentant la pressio o disminuint la pressió.
|
|
Activitats Moodle Nou
Positró 3 http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=2§ion=3 |
|
1) Selecciona. Estats d'agregació. Question 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1.6. Teoria cineticomolecular de la matèria
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=2§ion=4
|
|
Per poder explicar les propietats i el comportament dels diferents
estats d'agregació de la matèria (sòlid, líquid o gas) i també per explicar
com i perquè succeeixen els canvis d'estat, els científics han desenvolupat
una teoria, l'anomenada teoria cineticomolecular
de la matèria, que té com a postulats principals aquests: |
Postulats
de la teoria cineticomolecular
|
|
La matèria està
constituïda per partícules molt petites, pràcticament invisibles. Entre
aquestes partícules, hi ha el buit, és a dir, no hi ha res. En els sòlids, les partícules estan molt juntes, gairebé en contacte.
En els líquids hi ha més separació. En els gasos, la separació és molt gran. |
|
|
Les partícules exerceixen
entre si forces d'atracció que les mantenen unides. La intensitat de la força pot ser molt variada. En els sòlids, la
força d'atracció és molt gran; en els líquids, moderada; en els gasos, molt
petita, quasi inexistent. |
|
|
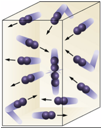
Les partícules estan en
moviment constant. Les
partícules dels sòlids quasi no es mouen. Et pots imaginar un sòlid com una
estructura de partícules unides entre si per una espècie de molles, de manera
que a penes poden vibrar (fig. 1). En els líquids es dóna una situació intermèdia. Les partícules que
formen un líquid es mouen més que les partícules dels sòlids, però menys que
les dels gasos. Les
partícules dels gasos es mouen independentment les unes de les altres, i es
desplacen per tot el volum del recipient que les conté (fig. 2). IMPORTANT: hem de tenir
en compte que com més elevada és la temperatura de la matèria, més gran serà
la velocitat del moviment de les partícules. Per això molts cossos es dilaten
amb la calor. |
|
|
|
|
|
Activitats Moodle Nou
Positró 3 http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=2§ion=4 |
|
1) Completa. Forces entre les partícules 2) Selecciona. La teoria cinètic-molecular de la
matèria |
|
1.7. Models atòmics
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=3
VÍDEOS: Atom. Models atòmics
ok-05. Atomo-part.subatomica-radioactividad.mp4 ok-06. Experimento de Rutherford-subtitulado.mp4 ok-07. MODELOS ATÓMICOS.mp4 |
1.7.1. De què està feta la
matèria? Les primeres teories dels grecs.
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=3
|
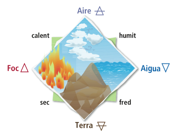
Al segle V a.C., és a dir, fa uns 2500 anys, alguns filòsofs creien que tot estava format per la combinació de quatre elements. Els quatre elements eren: aigua, aire, foc i terra. Era un teoria incorrecta però l'important era que s'intentava respondre la pregunta " De què està feta la matèria?" |
|
|
En aquell mateix segle, va aparèixer la primera hipòtesi de l'existència de l’àtom enunciada pels filòsofs grecs Demòcrit i Leucip. Aquesta hipòtesi deia que: La matèria era formada per unes partícules molt petites i indivisibles, els àtoms. Els àtoms eren les partícules més petites en què es podia dividir la matèria. Àtom
en grec vol dir "sense parts" |
|
|
|
Bitllet grec en homenatge a Demòcrit |
|
|
Llibre: Esas grandes preguntas. ¿De qué estan hechas las cosas? http://www.profefaro.com/3rESO/Quimica/atom-TP-enllac/imagenes/de-que-estan-hechas.jpg ¿Qué son los átomos? http://www.profefaro.com/3rESO/Quimica/atom-TP-enllac/imagenes/que-son-atomos.jpg |

1.7.2. La teoria atòmica de
Dalton
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=3
El 1808, el científic anglès
John Dalton (1766-1844) va publicar les seves idees sobre la constitució de la
matèria.
El postulat més important de la seva teoria deia que:
|
|
La matèria és formada per
partícules extremament petites, indivisibles i indestructibles anomenades
àtoms. L'àtom
és com una bola massissa, sense parts i indestructible |
|
|
|
Com va fer Dalton per deduir que existia l'àtom si no els podia
veure? Bé, Dalton va analitzar una sèrie de lleis sobre les reaccions
químiques i es va adonar que si suposava que la matèria està formada per
àtoms les lleis s'explicaven de forma natural. |
1.7.3. Model atòmic de
Thomson
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=4
Segons el model atòmic de Dalton, que acabem de veure, els àtoms eren
indivisibles i no tenien estructura interna. Això no obstant, el 1897, el físic britànic J. J. Thomson (1856-1940) va descobrir
una partícula que existia dins de l’àtom (partícula subatòmica), l'electró.
Thomson va descobrir que els electrons són partícules molt petites amb
càrrega elèctrica negativa i va proposar un model atòmic segons el nou
descobriment
Model atòmic de Thomson
|
|
Els àtoms estan formats
per electrons, amb càrrega negativa, que estan distribuïts per una esfera de matèria
de càrrega positiva. Com que hi tanta càrrega positiva com negativa l'àtom és
elèctricament neutre. L'àtom
de Thomson seria semblant a un pudding de panses, on les panses serien
electrons. |
|
|
|
Es va estimar la grandària d'un àtom i es va arribar a la conclusió
que tenia un diàmetre de prop de 10–10 m.
(10–10 m = 0,000 000 000 1 m) Perquè te'n facis una idea: en una línia d'1 cm de
longitud feta amb llapis hi ha uns 63 milions d'àtoms de carboni en filera: |
Origen de la paraula "electró"
La paraula "elektron" és la paraula grega per designar
l'ambre, la resina groga fòssil dels arbres de fulla perenne
|
|
|
|
|
|
|
|
|
|
|
|
1.7.4.Model atòmic de
Rutherford
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=4
L'any 1908, el físic Ernest
Rutherford (1871-1937) va dirigir un experiment que el van dur a elaborar un
altre model atòmic.
|
|
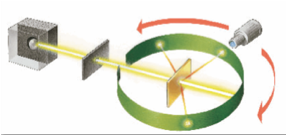
Experiment de Rutherford Es van llançar a gran velocitat unes partícules de grandària atòmica
( anomenades partícules alfa o raigs alfa) i amb càrrega positiva contra una
pel·lícula d'or molt fina. Un cop feta l'experiència, es van obtenir els
resultats següents: La majoria
de les partícules alfa travessava la làmina d'or sense desviar-se. Una petita
proporció de partícules travessava la làmina, però experimentava una petita
desviació. Una de cada
10.000 partícules alfa rebotava quan arribava a la làmina i tornava enrere. |
|
El resultat de l'experiència de la làmina d'or va sorprendre els
científics, que no es podien explicar que algunes partícules alfa, en xocar a
gran velocitat contra la làmina tan prima, sortissin rebotades. Rutherford va
dir que era «com si en disparar una bala contra un paper de fumar, en comptes
de travessar-lo, sortís rebotada». Per a Rutherford, aquest fet tan sols es podia explicar si la càrrega
positiva de l'àtom està concentrada en una part molt i molt petita de l'àtom
en comptes de trobar-se distribuïda per tot l'àtom, tal com suposava Thomson.
De manera que, quan les partícules alfa xoquen contra aquest punt de l'àtom
on es concentra la càrrega positiva, la repulsió entre càrregues del mateix
signe fa que surtin rebotades. En conseqüència, va idear el model atòmic següent: |
|
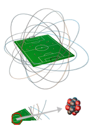
El
model de Rutherford,
|
|
-Els àtoms tenen dues
zones diferenciades: el nucli i l'escorça -El nucli és molt petit
comparat amb l'àtom però conté gairebé tota la massa i tota la càrrega
positiva. -Els electrons giren al
voltant del nucli en un espai molt més gran. -El nombre d'electrons
iguala la càrrega positiva del nucli i l'àtom és elèctricament neutre. |
|
|
|
Per fer-nos una idea: si l'àtom fos de la mida d'un camp de futbol, el nucli seria com el cap (1 mm de diàmetre) d'una agulla col·locada al centre del camp, i els electrons serien com puntes d'agulla que girarien al voltant seguint, aproximadament, els límits del camp. |
El
model atòmic de Bohr
El científic danès Niels Bohr (1885-1962) va fer un seguit d'estudis dels quals va deduir que els electrons no poden estar en qualsevol lloc de l'escorça sinó únicament en unes determinades òrbites circulars.
El
model atòmic actual
El model de l’àtom actualment és una mica complicat i no el tractarem en aquest curs.
És l'anomenat model mecanicoquàntic de l'àtom
-Se substitueix la idea que l'electró se situa en determinades capes o nivells per la probabilitat de trobar l'electró en una certa regió de l'espai, anomenada orbital. Un orbital és un lloc de l'espai on es molt probable trobar l'electró però no saben exactament la seva posició.
- També se substitueix la idea de que l'electró és com una bola donant voltes entorn del nucli. Ara s'accepta que l’electró es comporta com una bola donant voltes (matèria) però també és com
energia (una ona). D'això se'n diu la dualitat ona-corpuscle de l'electró.
|
|
Activitats Moodle Nou
Positró 3 http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=4 |
|
2) Ordena. Partícules subatòmiques |
|
Activitat
interactiva
|
Concurso.cnice.mec.es.
Aplicación web interactiva de los temas de química 3r ESO VERDADERO O FALSO? ELEMENTOS, COMPUESTOS, MODELOS ATÓMICOS http://concurso.cnice.mec.es/cnice2005/35_las_reacciones_quimicas/curso/em_ex01.html |
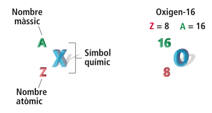
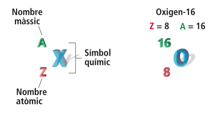
1.8. 3.1. Nombre atòmic i nombre màssic
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=5
|
VÍDEOS: Isotopes.mp4 APPLET: Taula periòdica de la PDI Smart.
(veure com varien els àtoms al
llarg de la TP) |
Els àtoms estan formats per protons, neutrons i electrons.
Per estudiar-los, definirem els conceptes de nombre atòmic i nombre màssic:
|
|
El
nombre atòmic, Z, és el
nombre de protons que té un àtom. Tots els protons de l'àtom es troben al nucli. |
|
El
nombre màssic, A, és la
suma del nombre de protons i el nombre de neutrons. |
|
|
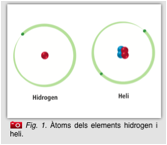
Un element químic es caracteritza perquè tots els àtoms tenen, al nucli, el mateix nombre de protons. Per exemple, l'hidrogen té 1 protó; l'heli, 2; l'oxigen, 8; el carboni, 6 i l'urani en té 92 |
|
Si al nombre atòmic A li restem nombre màssic Z el resultat és el nombre de neutrons (N): A – Z = N |

3.2. Isòtops
|
Construeix un àtom http://www.educaplus.org/play-74-Constructor-de-%C3%A1tomos.html |
S'ha comprovat que hi ha àtoms d'un mateix element químic que tenen masses diferents. Per exemple un àtom d'or pot tenir una massa diferent d'un altre àtom d'or
Això significa que el nombre de partícules en aquests àtoms ha de ser diferent.
Com que el nombre de protons és fix i la massa dels electrons ínfima (quasi zero), és el nombre de neutrons el que ha de ser diferent.
|
Els isòtops són aquells àtoms que tenen el mateix nombre atòmic, però diferent nombre màssic. O sigui, que tenen el mateix nombre de
protons però diferent nombre de neutrons |
|
|
Per identificar els isòtops d'un mateix element utilitzem una notació simbòlica en què s'indica, a més del símbol de l'element, el nombre atòmic i el nombre màssic El nombre màssic A s’afegeix com superíndex a l'esquerra. El nombre atòmic Z s’afegeix com subíndex a l'esquerra |
Per tant, el carboni-12 (6 protons i 6
neutrons) el simbolitzem ![]() ,
,
l'oxigen-16 (8 protons i 8 neutrons) el
simbolitzem ![]()
|
|
Activitats Moodle Nou
Positró 3 http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=4§ion=5 |
|
1) Completa. Protons, neutrons i electrons (Indica
el nombre de protons, neutrons i electrons dels isòtops següents:) |
|
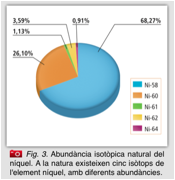
Abundància
isotòpica natural
|
|
La majoria dels elements químics estan formats per més d'un isòtop. El percentatge de cadascun dels isòtops que hi ha a la natura formant un element és l'abundància isotòpica natural de l'element. |
L'urani té nombre atòmic Z =92.
L'urani natural està format per tres tipus d'isòtops amb nombre màssic A = 238, 235 i 234:
urani-238 (238U)
urani-235 (235U)
i urani-234 (234U).
De cada gram d'urani natural el 99'28 % de la massa és urani-238, el 0'71% és urani-235 i el 0'005% és urani-234.
La proporció entre urani-238 i urani-235 és la mateixa a tota la Terra i a la resta dels planetes del sistema solar.
El seu isòtop urani-235 és usat com a font d'energia en els reactors nuclears i les armes nuclears
1.9. Enllaç químic
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=5
Nota
MIF: A 3R ESO es pot explicar l'enllaç iònic, covalent
i metàl·lic. L'alumne dedueix els tres tipus d'enllaços utilitzant boles de
plàstic i el concepte d'aconseguir l'octet. Dedueix amb facilitat si s'han de
compartir o cedir els electrons.
VÍDEO: Enllaç
Ionic and covalent bonding animation.mp4 |
|
Nota:
per
trobar imatges d'àtoms amb electrons a les capes mireu http://chemistry.about.com/od/elementfacts/ig/Atom-Diagrams/Sodium-Atom.htm |
|
|
Veure
animacions de diferents enllaços iònics: http://www.educaplus.org/play-77-Enlace-i%C3%B3nico.html |
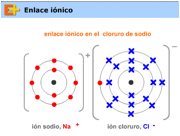
Els àtoms s’uneixen
uns amb altres a través d’enllaços
Per què s’uneix un àtom amb un altre àtom?
D’una forma molt resumida direm que és perquè els àtoms volen tenir 8 electrons en la seva última capa de l’escorça ja que això els dóna estabilitat.
Quan un àtom té 8 electrons en la última capa es diu que té l’octet complet
Veiem un exemple:
El sodi Na té 1 electró en la seva capa més externa i 8 electrons en la seva segona capa.
Si dóna l’electró de la capa més externa es quedarà amb vuit electrons en la segona capa.
Així ja tindrà 8 electrons en la última capa i estarà estable
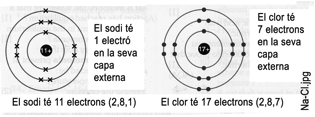
El Clor Cl té 7 electrons en la seva capa més externa. Si agafa 1 electró i el posa a la capa més externa, es quedarà amb vuit electrons per tant ja tindrà 8 electrons en la última capa i estarà estable

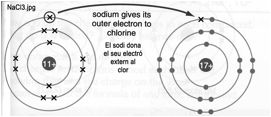
Per tant,
• El sodi Na vol
donar 1 electró
• El Clor Cl vol
agafar 1 electró
Si es troben 1 àtom de Na i 1 àtom de Cl, el Na li dona 1 electró al Cl i s’uneixen mitjançant un enllaç.
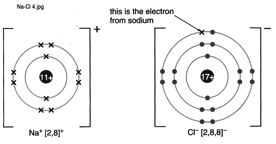 D’aquí que la fórmula del clorur de sodi sigui NaCl ( un àtom de Na amb 1
àtom de Cl)
D’aquí que la fórmula del clorur de sodi sigui NaCl ( un àtom de Na amb 1
àtom de Cl)

1.10. La taula periòdica
LINK: Educaplus.org
http://www.educaplus.org/sp2002/properiodicas/radatomico.html
VIDEO: Taula periòdica
ok-02.¿De qué estamos hechos_.mp4 ok-Mendeleiev_una_taula_digna_d_un_nobel.flv Chemical Party.mp4 APPLET: Taula periòdica de la PDI Smart.
(veure com varienles capes i
nuclis dels àtoms al llarg de la TP) |
1.7.1. Els elements químics.
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=3
Ja hem vist abans que els materials formats per un sol tipus d'àtom es denominen «elements». Son elements, per exemple, l'or (Au), la plata (Ag), l'oxigen (O), l'hidrogen (H), el ferro (Fe).
1.1. Els elements a la
natura
Coneixem més d'un centenar d'elements.
A la natura podem trobar-n'hi només 90, els anomenats elements naturals; la resta han estat creats als
laboratoris de física i reben el nom d'elements artificials (fig. 1).
Hi ha pocs elements naturals que podem trobar en estat lliure, ja que
gairebé tots es troben a la natura combinats amb altres formant compostos.
Els elements a la Terra
L'element que més abunda al nostre planeta és el ferro, encara que no és el més abundant al nostre voltant ja que la
major part d'aquest element es troba al nucli terrestre.
El silici és el segon element
més abundant de la escorça terrestre (suposa el 25.7% del seu pes) després de
l'oxigen. Apareix en l'argila, el feldspat, granit, quars i sorra,
principalment en forma de diòxid de silici SiO2 (també conegut com
sílice) i silicats (components que contenen silici, oxigen i metalls). El
silici és el component principal del vidre, ciment, ceràmica, la majoria de
silicones (substància plàstica).
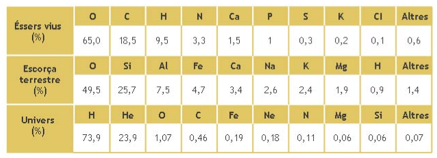
Els elements en els éssers
vius
En els éssers vius, el 99% de la matèria és constituïda únicament per
sis elements:
oxigen, carboni, hidrogen,
nitrogen, calci i fòsfor (CHONCaP)
L'1% que resta correspon a una gran diversitat d'elements, alguns en
quantitats mínimes, però que són indispensables perquè les funcions biològiques
es facin correctament. Aquests elements són els anomenats oligoelements, com el
cobalt, el coure, el zinc, el seleni o el fluor, etc.
Els elements a l'univers
Els elements més abundants de l'univers són els més lleugers: l'hidrogen i l'heli.
Aproximadament, el 90% de tots els àtoms de l'univers són d'hidrogen,
el 9% són d'heli i l'1% que resta correspon a altres elements

1.2. Taula periòdica dels elements
Al segle XIX, el descobriment progressiu de nous elements químics va
dur els científics a intentar classificar-los per així facilitar-ne l'estudi.
El químic rus Mendeleiev va fer una ordenació periòdica dels elements
que és la precursora de la que fem servir avui dia.
El 1869, Mendeleiev va publicar una taula dels elements on va col·locar
els 63 elements que es coneixien llavors i els va ordenar en fileres i en
columnes (fig. 5). Mendeleiev va reservar espais buits per a elements que
encara no havien estat descoberts. Amb el temps, aquests elements es van anar
descobrint i tenien les propietats que havia predit Mendeleiev
Ekasilici significa ‘sota el silici’,
correspon al germani, Ge.
Ekabor significa ‘sota el bor’, correspon a
l’escandi, Sc.
Ekaalumini significa ‘sota l’alumini,
correspon al gal.li, Ga.
La taula dels elements que utilitzem en l'actualitat, anomenada taula periòdica deriva d'aquella
primera del 1869,
|
En la taula periòdica
actual els elements s'hi ordenen en
ordre creixent de nombre atòmic Z. |
2. Els elements a la taula
periòdica
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=4
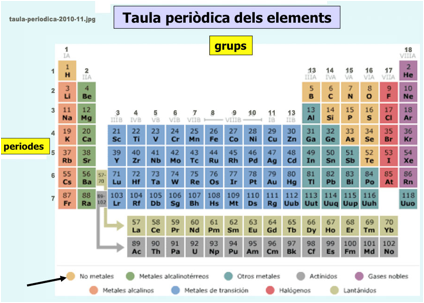
2.1. Grups i períodes
A la taula periòdica actual, els elements estan col·locats en ordre
creixent de nombre atòmic
|
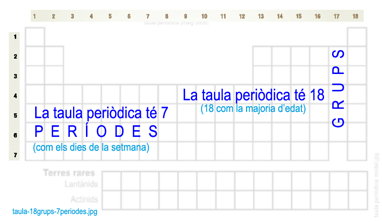
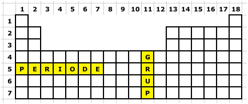
La taula periòdica actualment té 118 elements (febrer 2012) Es troben disposats en 18 grups i 7 períodes. |
Els grups s'identifiquen amb les columnes (en
vertical) de la taula periòdica
i els períodes, amb les fileres (en
horitzontal).
Cada grup conté elements amb propietats semblants. Per exemple en el grup 18 (gasos nobles)
el He, Ne, Ar, Kr. Xe, Rn tots els elements s'hi assemblen en propietats. Igual
passa, per exemple, amb els alcalins (grup 1) Li, Na , K, Rb... etc.
Alguns dels grups de la taula periòdica tenen noms distintius. Citarem
tres grups molt coneguts:
Alcalins. Són els elements del grup 1
(tret de l'hidrogen).
Halògens. Són els elements del grup 17.
Gasos nobles. Són els elements del grup
18. Els anomenem així perquè són extraordinàriament estables i quasi no es
combinen amb altres elements.
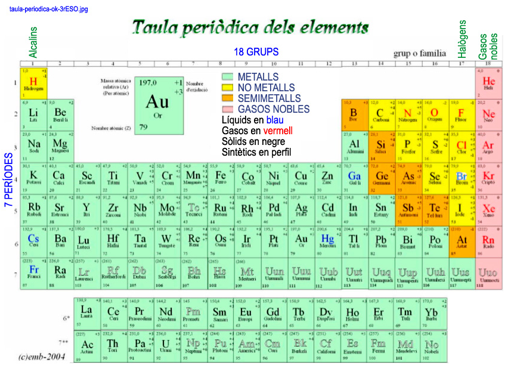
Metalls,
no metalls i semimetalls
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=4
En funció del caràcter metàl·lic podem classificar els diferents
elements en tres famílies:
Metalls. (en verd a la taula periòdica de dalt) Tenen
un aspecte relluent (brillantor metàl·lica) i estan freds quan els toquem,
perquè són molt bons conductors de la calor.
Els metalls també
són bons conductors de l'electricitat (l'argent és el millor), mal·leables (els
podem donar forma de làmines) i dúctils (els podem donar forma de fil)
No-metalls. (en groc a la taula periòdica de dalt) No
tenen propietats metàl·liques. Molts d'aquests són gasos, com l'oxigen i el
nitrogen, però també n'hi ha que tenen el punt de fusió força elevat, com el
carboni.
Els agrupem a
la dreta a la taula periòdica.
Semimetalls. (en taronja a la taula periòdica de dalt)
Són elements difícils de classificar, perquè tenen característiques intermèdies
entre els metalls i els no-metalls.
Alguns
semimetalls, com el silici i el germani, els utilitzem per a la fabricació de
components electrònics.
Els elements de la taula periòdica també s'agrupen en:
Elements representatius (en verd)
Elements de transició (en vermell)
Elements de transició interna (en crema)

|
Noms d'alguns grups i
períodes |
|
|
Propietats
periòdiques. El volum atòmic
http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=4
Algunes de les propietats dels elements canvien de forma amb
regularitat dins d'un grup o un període.
En aquest curs només parlarem d'una propietat periòdica: el volum de
l'àtom
|
|
El volum dels àtoms disminueix
en desplaçar-se d'esquerra a dreta en un període El volum dels àtoms augmenta en
baixar en un grup |
|
|
Taula periòdica amb la grandària dels àtoms: http://www.profefaro.com/LINKS-INFO/imagenes/tamany.atoms.TP.jpg |
|
|
Activitats Moodle Nou
Positró http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=4 |
|
1) Selecciona. Caràcter metàl·lic. Indica si els elements químics següents són
metalls, semimetalls o no metalls: 2) Ordena. Volum atòmic relatiu. Ordena de menys a més volum atòmic els àtoms
dels elements següents: 3) http://centres.vicensvivesdigital.cat/35099/course/format/vvives/unit.php?id=18&unit=5§ion=7 Selecciona. Característiques dels metalls |
|